
 期刊:Science immunology
期刊:Science immunology
影响因子:16.3
伯豪技术服务+产品:单细胞测序、伯优®组织样本悬液制备试剂盒
研究背景
先天淋巴细胞(ILCs)作为天然免疫的关键组成部分,在抗感染、免疫调节和组织重塑中发挥核心作用。然而,胚胎期与成体骨髓造血如何时空性贡献于ILC库的问题长期存在争议。本研究通过谱系追踪、单细胞测序和移植实验等技术,揭示了 ILCs 的双起源模式:髓外ILCs起源于胎儿肝脏(FL)产生的 PD-1⁺ILC 前体(ILCPs),这些前体在胚胎期定植于肺、肠道等外周组织,在局部微环境诱导下分化为双能 ILC1/ILC3 前体(ILC1/3P)或 ILC2 前体(ILC2P),并终身维持组织 ILC 库,且不依赖成体骨髓造血;髓内ILC2s主要依赖骨髓造血。该研究首次系统阐明了 ILCs 的发育动力学,为理解天然免疫细胞的胚胎起源与组织维持机制提供了全新框架,对感染、炎症等疾病的靶向治疗具有重要启示。
关键技术
单细胞测序、伯优®组织样本悬液制备试剂盒
(技术服务及科技产品由伯豪生物提供)
研究结果
1. 胚胎期 ILC 前体的时空出现规律
众所周知,先天淋巴细胞家族起源于表达α4β7的祖细胞(αLPs),且在 αLP 群体中已发现多种先天淋巴细胞谱系限制性祖细胞。研究首先通过流式细胞术追踪了胚胎期 α4β7⁺淋巴样前体(αLPs,ILCs 的发育前体)的分布。结果显示,αLPs 最早在 E12.5 的胎儿肝脏中被检测到,而此时胎儿肺和肠道中尚未出现;E13.5 时,肺和肠道中出现 αLPs,且其中绝大多数为 PD-1⁺ILCPs(经典 ILC 前体标记)。这一时间差提示,PD-1⁺ILCPs 可能起源于胎儿肝脏,并随后迁移至外周组织。
进一步通过 Fgd5 谱系追踪模型(标记造血干细胞及其后代)证实:E12.5 时胎儿肝脏的造血干细胞(HSCs)被标记后,E18.5 时肝脏、肺和肠道的 ILCPs 均携带相同标记,且标记效率与胎儿肝脏 HSCs 一致。这直接证明,外周组织的 ILCPs 均来源于胎儿肝脏 HSCs,而非卵黄囊(YS)等其他胚胎造血位点(卵黄囊中未检测到 αLPs)。
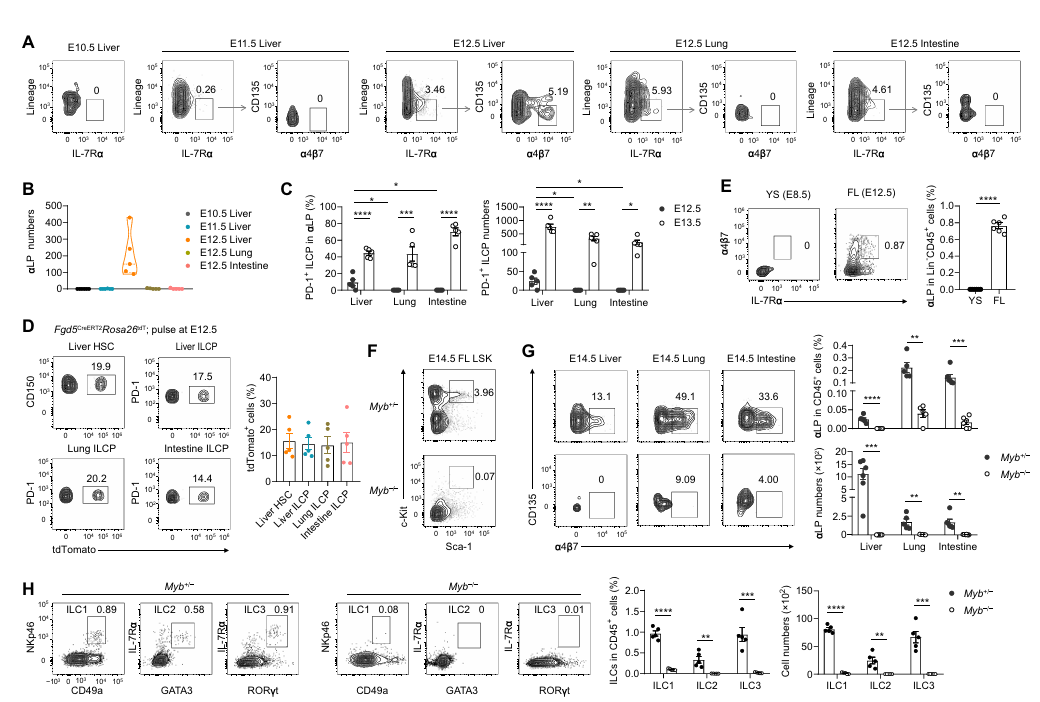
图1. 胎儿肝脏造血干细胞来源的 ILCP 在胎儿发育期间定植于外周组织
2. 胎儿肝脏 ILCPs 的异质性与发育轨迹
为解析胎儿肝脏 ILCPs 的分子特征,作者对E14.5胎儿肝脏的αLPs进行了scRNA-seq。聚类分析显示,这些细胞可分为 5 个亚群,其中 C4 亚群高表达 Tcf7、Lef1 等基因,符合早期先天淋巴样前体(EILPs)特征;C1 亚群表达 Pdcd1(PD-1)、Zbtb16(PLZF)等,为 PD-1⁺ILCPs;C2 亚群高表达 Klrd1(CD94),后续被证实为双能 ILC1/3P;C3 亚群表达 Lta、Il22 等,为 ILC3 前体(ILC3P)。
拟时序分析进一步揭示了其发育路径:EILPs(C4)→PD-1⁺ILCPs(C1)→CD94⁺ILC1/3P(C2)→ILC3P(C3),形成连续的分化层级。这一发现不仅明确了胎儿肝脏 ILCPs 的内部结构,还为后续组织特异性分化奠定了基础。
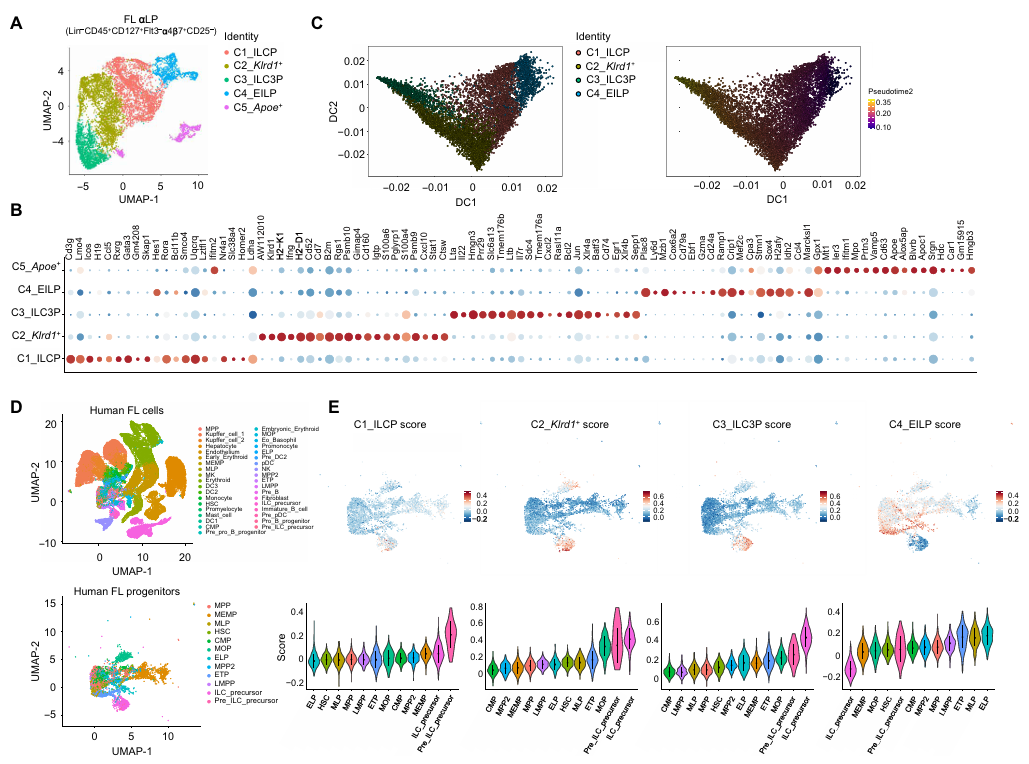
图2. 胎儿肝脏先天淋巴细胞祖细胞的异质性和发育轨迹
3. CD94 标记双能 ILC1-ILC3 前体,位于 ILCPs 下游
scRNA-seq 鉴定的 C2_Klrd1⁺群体(表达 CD94)引起关注。研究发现,胎儿肝脏中部分 αLPs 表达 CD94,这些 CD94⁺前体多为 CD160⁺PD-1⁻,低表达 Zbtb16,高表达 NKG2A、CD49a 等分子,且转录因子调控网络显示其表达 Tbx21 和 Rorc,可能与 ILC1 和 ILC3 发育相关。通过 Klrd1 命运图谱模型和体外培养实验证实,CD94⁺前体可生成 ILC1 和 ILC3,但不生成 ILC2 和 cNK 细胞,故将其定义为双能 ILC1-ILC3 前体(ILC1/3Ps)。常规转录组测序和功能实验进一步表明,ILC1/3Ps 的转录谱与 ILCPs 更接近,且由 ILCPs 直接分化而来,是 ILCPs 的下游后代。
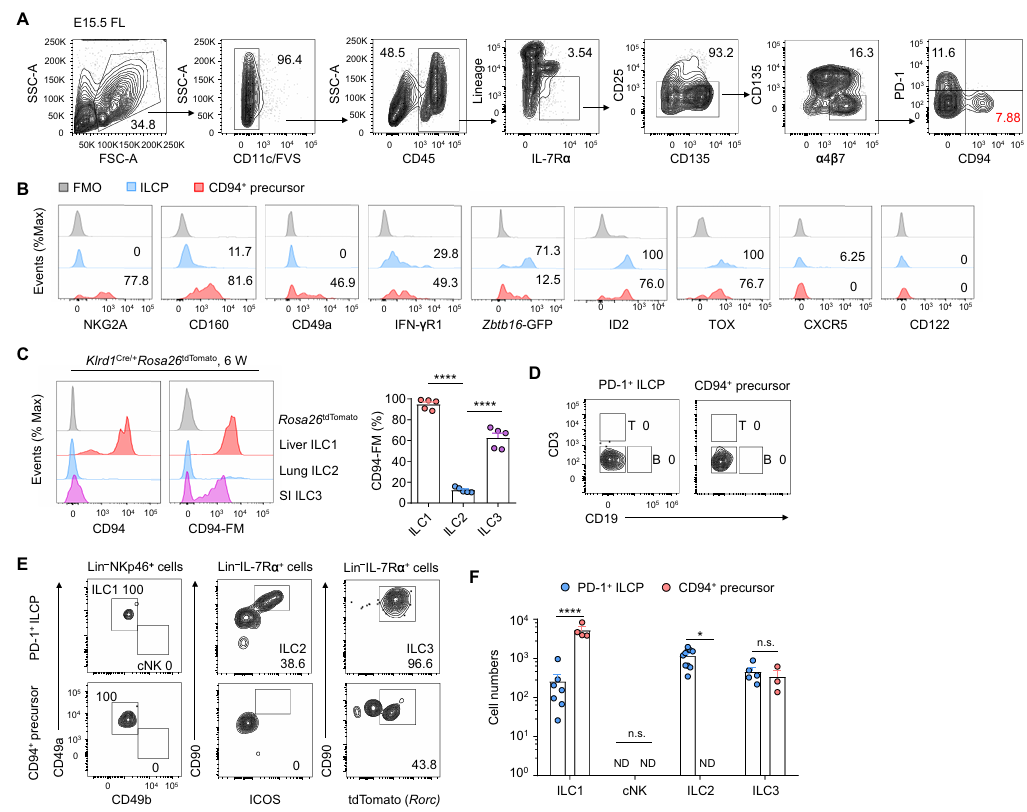
图3. CD94⁺前体生成 ILC1 和 ILC3
4. 组织微环境引导 ILCPs 向特定先天淋巴细胞亚群分化
对胎儿至成年期组织中先天淋巴细胞祖细胞的分析显示,ILCPs 数量在胎儿期或新生儿期达峰,成年后极少;ILC1/3Ps 和 ILC2Ps 的比例因组织而异:肝脏以 ILC1/3Ps 为主,成年后 ILC1 占成熟亚群主导;肺中 ILC2Ps 随发育增加,成年后 ILC2 占优;肠道中两种前体均持续存在,ILC3 占成熟亚群 60%。这种前体与成熟细胞的比例匹配,暗示组织微环境的定向调控作用。过继转移实验证实,胎儿肝脏 ILCPs 在肝脏中主要分化为 ILC1,在肺中为 ILC2,在肠道中则涵盖所有亚群;而 ILC1/3Ps 仅能生成 ILC1 和 ILC3,失去 ILC2 潜能。这表明组织微环境决定了 ILCPs 的分化偏好。
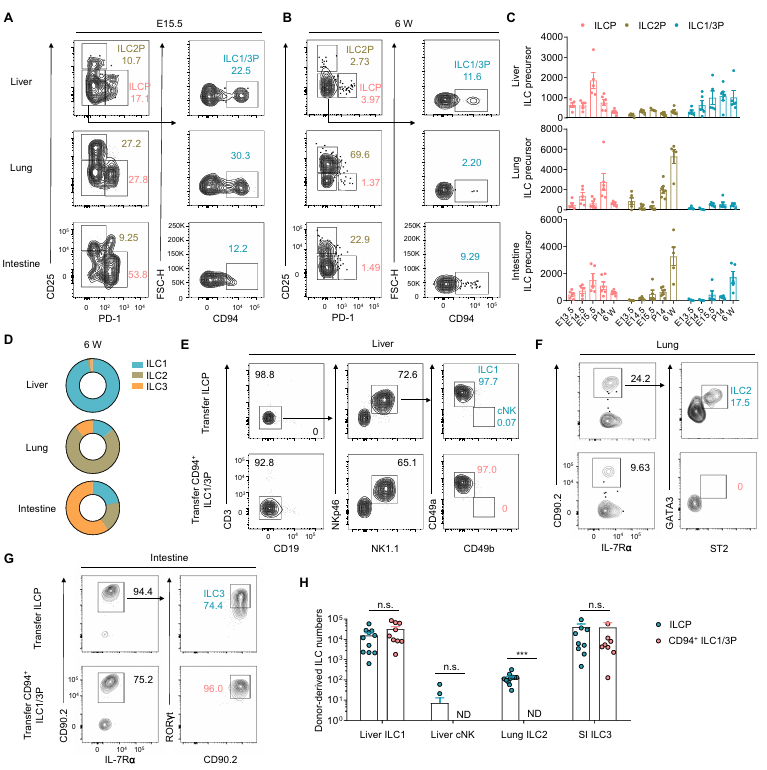
图4. 不同的组织微环境促使 ILCP 生成不同的先天淋巴细胞亚群
5. 多数外周先天淋巴细胞的发育与扩增不依赖骨髓造血
出生后骨髓虽为主要造血器官,但对先天淋巴细胞的贡献有限。Fgd5 命运图谱分析显示,成年后外周组织 ILC1/3Ps、ILC2Ps 及成熟先天淋巴细胞的骨髓来源标记率极低,归一化后超 80% 的髓外先天淋巴细胞起源于胚胎前体,与骨髓无关。骨髓移植实验也证实,供体骨髓仅能重建 30% 的 cNK 细胞,对 ILC1、ILC2、ILC3 的重建率仅 2%~6%。
病理状态下,LCMV 感染、IL-33 诱导的肺炎症及柠檬酸杆菌感染均会诱导组织内 ILC 前体局部增殖(如肝脏 ILC1/3Ps 增殖率从 10.7% 升至 15.8%),而非依赖骨髓来源的新细胞,进一步证实外周先天淋巴细胞的自主维持特性。

图5. 外周先天淋巴细胞的发育不依赖骨髓造血干细胞
6. 骨髓造血对髓内 ILC2 发育至关重要
与髓外不同,骨髓中先天淋巴细胞祖细胞以 ILC2Ps 为主(占 97.2%),scRNA-seq 显示 pre-ILC2Ps 在骨髓中显著富集。命运图谱分析表明,骨髓 ILC2Ps 和成熟 ILC2s 的标记率与骨髓 HSCs 一致(超 60%),归一化后超 80% 的骨髓 ILC2s 由髓内造血生成,而外周 ILC2s 中骨髓来源不足 20%。这表明骨髓造血主要支持髓内 ILC2s 的发育,可能与骨髓脂肪微环境的调控有关。
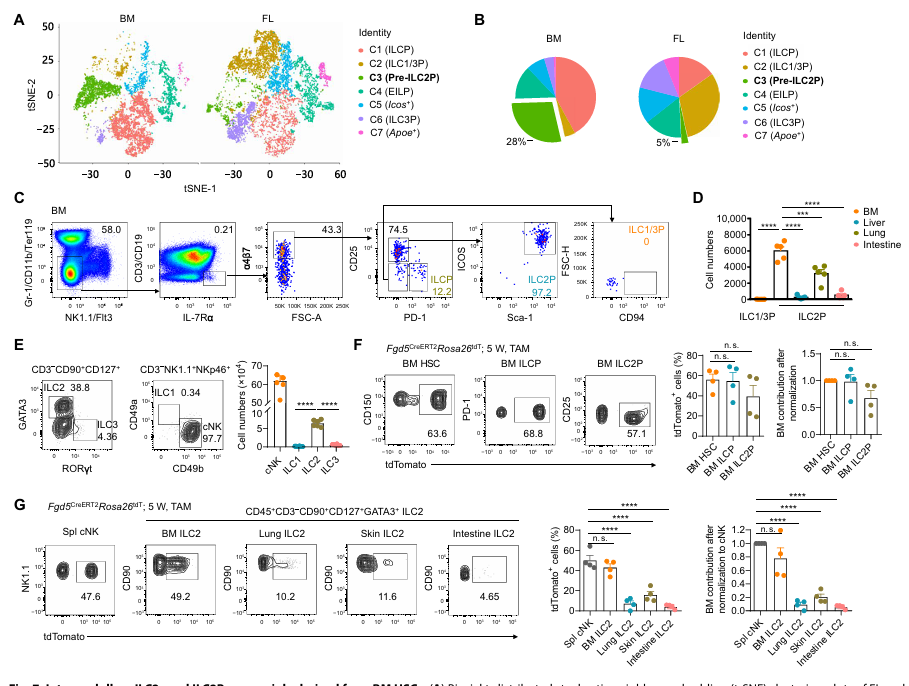
图6. 骨髓内 ILC2 和 ILC2 前体主要来源于骨髓造血干细胞
参考文献:
[1] Wang X, Li J, Rebuffet L, Cheng M, Bao B, Chen Y, Zheng X, Chen Y, Sun H, Sun R, Vivier E, Peng H and Tian Z 2025 Innate lymphoid cells originate from fetal liver-derived tissue-resident progenitors Sci Immunol 10 eadu7962
伯优®组织样本悬液制备试剂盒
本产品适用于多种组织样本的单细胞悬液制备。组织样本预处理后利用酶温和、快速、有效地破坏细胞外基质,释放细胞,经过筛、离心等标准化操作流程,生成高质量的单细胞悬液。实验操作简单便捷,不需要特别的解离仪器,可轻松实现多种组织的解离。制备的单细胞悬液可用于单细胞测序、细胞培养或其他细胞相关检测。
本产品适用于胃、肾、肺、心脏、肝、肠、甲状腺、胸腺、食管、鼻组织、皮肤、黏膜、胚胎、淋巴、睾丸、乳腺、卵巢、肿瘤组织等样本(软骨、硬骨、脂肪、胰腺、脑组织除外)。
